Archivo
Investigadores suizos trabajan en el desarrollo de vacunas terapeúticas contra el cáncer
Los profesionales del Instituto Ludwig, de Lausana, buscan soluciones para los tumores que resisten quimioterapia y radioterapia.

DESCARGA LA APP EL TIEMPO
Personaliza, descubre e informate.
Nuestro mundo

El pueblo que en el pasado reunió a todas las tribus y aún conserva su arquitectura
El pueblo se erige sobre la sierra con una vista única hacia las montañas de la región.

El pueblo a 1 hora de Bogotá en auto que tiene calles coloniales y un buen café
Un sabroso café de origen y las distintas actividades lo convierten en uno de los mejores pueblos.

Impactantes videos | Fuertes lluvias generan emergencia en Dubái; vuelos fueron cancelados
Además, en Omán hay al menos 18 personas fallecidas producto de la situación por las precipitaciones.

Irán e Israel, de aliados a enemigos jurados: los hechos que han marcado la tensión entre ambos países
Estos es lo que ha pasado entre ambos países en las últimas décadas.

Reportan incendio forestal en cerro del sur de Bogotá, en plena crisis por el agua
El Alcalde hizo un llamado a evitar las quemas y fogatas en la ciudad.

Comerciante denuncia que le robaron millonaria suma en Bogotá: lujosa camioneta quedó destruida
Los delincuentes fueron capturados.

Director de la UNGRD anuncia trabajo articulado para disminuir riesgos en Hidroituango
Carlos Carrillo visitó la central junto con Andrés J. Rendón, Federico Gutiérrez y John Maya.

Medellín: denuncian 13 casos de presunta corrupción en el Área Metropolitana
Paula Palacio alertó posibles irregularidades en contratación durante la administración anterior.

Lo último: Bomberos de Cali logran controlar incendio forestal en La Buitrera
Al menos 30 unidades buscan que la conflagración no llegue a viviendas aledañas.

Rescatan en Candelaria a una mujer que habría sido secuestrada por su exempleado
Captores exigían cerca de 600 millones de pesos por su liberación.

Los billares y casinos que fueron cerrados en Barranquilla por robo de energía
Las pérdidas mensuales ascienden a los más de 250 millones de pesos.

El río Magdalena, patrimonio cultural y comercial que agoniza por el abandono
Pese a haber sido declarado como sujeto de derechos, se necesitan acciones urgentes para su preservación y legado.

Atracan joyería en el Centro Histórico de Cartagena a pleno mediodía
Asaltantes se hicieron pasar por turistas, cinco de los delincuentes fueron capturados en Marbella

Fuerte accidente en la vía Ibagué-Líbano: reportan ocho personas heridas
Una posible falla en el sistema de frenos habría ocasionado la emergencia.

Argentina: Javier Milei ya no viajará en vuelos de aerolíneas comerciales para no arriesgar su seguridad
La decisión, según el portavoz presidencial, se dio tras una sugerencia del Ministerio de Seguridad.

Chile: los escándalos que ponen en jaque a sus dos principales cuerpos de seguridad
Casos de corrupción y acusaciones por violación de derechos humanos salpican a la Policía y los Carabineros.

Elecciones en Venezuela: el antichavismo se declara en 'reunión permanente' para definir candidatura de la oposición
Las organizaciones políticas que conforman la Plataforma Unitaria Democrática sostuvieron este martes una reunión.

(Video) Nicolás Maduro y su curioso inglés en mensaje a Joe Biden: 'If you want, I want'
En medio de su intervención en televisión pública el mandatario venezolano envió un mensaje en inglés a su homólogo en Estados Unidos.
Nicolás Maduro anuncia el cierre de todas sus sedes diplomáticas de Venezuela en Ecuador

'Venezuela seguirá su marcha económica con o sin licencias de EE. UU.': Maduro ante posible regreso de sanciones

¿Por qué Venezuela insiste en que el Tren de Aragua no existe y que es una 'ficción creada por la mediática internacional'?


'No permitiré que ningún jurado sea intimidado', advierte juez del caso penal contra Trump
El expresidente habría hecho gestos durante la interrogación de uno de los jurados, según el magistrado.

Alerta en EE. UU.: piloto voló un avión 'fabricado por aficionados' y se estrelló
El hecho tuvo lugar en la zona rural de Pensilvania, cuando la aeronave impactó en una granja local.

Las impactantes imágenes del incendio en Copenhague que arrasó con la antigua bolsa de valores
Aunque había personas en el edificio cuando inició la emergencia, no se reportan heridos.

Rusia: La advertencia que le lanzó Vladimir Putin a Irán por la confrontación con Israel
El presidente ruso alertó que una escalada tendría 'consecuencias catastróficas'. Teherán le respondió.

Moderna suspende el plan para construir en Kenia una fábrica de vacunas para África
Moderna pretendía producir en esa planta hasta 500 millones de dosis de vacunas al año para África.

Bailarín colombiano, de 21 años, murió en Egipto tras presentar fuerte dolor de cabeza: esto se sabe
La agencia de baile con la que viajó el joven no se ha pronunciado frente a la posible negligencia.

Sigue tensión en Oriente Próximo: Israel promete responder al ataque de Irán, que a su vez reitera amenazas
Los pronunciamientos se dan en medio de los llamados a la moderación de la comunidad internacional, que teme una escalada del conflicto en la región.

Israel prepara evacuación de civiles en Rafah para dar inicio a su invasión en el sur de Gaza
Fuerzas israelíes sostienen que la incursión permitirá eliminar distintos batallones de Hamás que se esconden en la zona.
Jefe del Estado Mayor de Israel asegura que habrá una 'respuesta' al ataque de Irán

Tras el ataque de Irán, Israel bombardea Gaza mientras el mundo pide calma en Oriente Próximo

Diplomacia y advertencias: así es cómo Irán busca contener las repercusiones de su ataque contra Israel

EN VIVO | Estados Unidos dijo que Irán no les informó sobre el ataque a Israel: 'Esta noción es ridícula'

Irán afirma que capturó buque vinculado a Israel por violación de las normas marítimas

Cuatro soldados israelíes heridos por una explosión en la frontera norte de Israel

Israel evalúa cómo responder tras el ataque masivo iraní: ¿qué opciones hay sobre la mesa?

Así son los misiles y drones que Irán usó para atacar a Israel
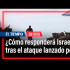
Estos son los aliados de Irán en Oriente Medio que también desafían a Israel

Así funciona la 'Cúpula de hierro', el principal escudo que utilizó Israel contra los ataques de Irán

Israel asegura que interceptó el 99 % de los misiles y drones iraníes: este es el balance de ambos países

Papa Francisco pide cesar la violencia tras ataque de Irán a Israel: 'Sigo en oración, con preocupación y también dolor'

Israel bombardea Líbano en medio de la creciente tensión tras el ataque iraní

¿Por qué Irán lanzó una lluvia de misiles y drones contra Israel y qué puede pasar tras el ataque?

El peligroso precedente que sientan los recientes ataques a cuerpos diplomáticos

Más de 200 drones y misiles disparados contra Israel: el balance preliminar del ataque iraní

Consejo de Seguridad de la ONU se reunirá este domingo tras ataque de Irán a Israel

Irán e Israel, de aliados a enemigos jurados: los hechos que han marcado la tensión entre ambos países


Video: pareja millonaria lanza todo el dinero de su fortuna a la calle para 'desprenderse de lo material'
La pareja de esposos, de India, repartió toda su fortuna como parte del proceso para convertirse en monjes.

Daniel Sancho, muy molesto con su abogado tailandés: costumbre local lo enfurece
Daniel Sancho comentó que no está conforme con su traductora y su abogado.
Juicio Daniel Sancho: abogado de Arrieta revela qué pasaría si pide perdón a la familia

Rayos y lluvias torrenciales en Pakistán dejan como saldo más de 20 muertos

Jaque mate al Hong Kong que fue

Hong Kong investiga caso de infección de zika y dengue en viajero procedente de Tailandia

Condenan a pena de muerte a magnate vietnamita por uno de los mayores fraudes

Vietnam condena a muerte a millonaria empresaria por fraude masivo de 27.000 millones de dólares

El juicio contra Daniel Sancho continúa con los testimonios de la Policía este 11 de abril

Japón busca ampliar alianzas de seguridad con Estados Unidos para hacer frente al 'expansionismo chino'

Juicio contra Daniel Sancho por asesinato de Edwin Arrieta: La compra de cuchillos y el alquiler de un kayak

Rodolfo Sancho pide 'respeto' durante su asistencia en juicio de su hijo, Daniel Sancho

Alrededor de 11 muertos dejó un accidente de un bus en una mina en el centro de la India

Incendio en edificio residencial de Hong Kong deja al menos 5 muertos y más de 20 heridos

A puerta cerrada y sin medios: las claves del inicio del juicio contra Daniel Sancho por asesinato del colombiano Edwin Arrieta

Rodolfo Sancho contó cómo se enteró de que su hijo Daniel había asesinado a Edwin Arrieta

China y Rusia: puntos claves del encuentro del presidente Xi Jinping y el canciller Serguéi Lavrov

Equipo chino trasplanta con éxito riñón genéticamente modificado de cerdo a cuerpo humano
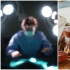
El juez encargado del caso de Edwin Arrieta prohíbe que se informe sobre el juicio

Comenzó juicio en Tailandia contra Daniel Sancho, presunto responsable del asesinato de Edwin Arrieta


Los náufragos rescatados en una isla desierta tras escribir 'HELP' en la arena de una playa
Se perdieron cuando iban camino a una isla deshabitada cerca de Guam, en donde otros marinos han sufrido la misma suerte.

El científico que estudia a las personas que poco antes de morir 'ven' a seres queridos que ya fallecieron
Este profesional es un médico y neurocientífico que afirma que al final de sus vidas, las personas tienen visiones sobre sus seres amados.
Qué fue de las 276 niñas secuestradas por el grupo militante islamista Boko Haram hace una década

Ataques a cuchillo y terrorismo en Australia: ¿qué hay detrás de los hechos violentos en Sídney?

China apoyaría una conferencia de paz 'reconocida por Rusia y Ucrania', dice Xi a Scholz

Ataque en iglesia de Sídney fue un acto terrorista, según policía australiana

Nuevo caso de violencia en Australia: un sacerdote y varias personas apuñaladas durante una misa en Sídney

Policía identifica al autor del apuñalamiento en un centro comercial en Sídney: ¿qué se sabe?

La Unión Europea condena enérgicamente el 'inaceptable' ataque de Irán contra Israel

Videos: así fueron los momentos de pánico en Sídney, Australia, cuando atacante persiguió a víctimas

Lo que se sabe sobre el ataque con cuchillo en Sídney en el que murieron seis personas

Al menos cinco personas mueren apuñaladas en un centro comercial en Australia

Estas son las increíbles nuevas pinturas de 2.000 años de antigüedad encontradas en Pompeya

Científicos identifican un posible brote de gripe aviar letal en la Antártida
Visados de oro: ¿en qué países se puede acceder a este mecanismo para obtener la residencia?

¿Viviría y trabajaría en Nueva Zelanda? Conozca la nueva normativa, según inmigración

Cuál es el origen de la rivalidad entre Israel e Irán y cómo la guerra en Gaza la está intensificando

5 ciudades turísticas que están haciendo del mundo un lugar mejor al ser sostenibles

Histórico: Consejo de Derechos Humanos de la ONU aprueba resolución sobre la intersexualidad, ¿de qué trata?

'No es broma': por qué Botsuana amenaza con enviar 20.000 elefantes a Alemania

Horóscopo
Encuentra acá todos los signos del zodiaco. Tenemos para ti consejos de amor, finanzas y muchas cosas más.
Crucigrama
Pon a prueba tus conocimientos con el crucigrama de EL TIEMPO


















































%20(2).jpg)


